Z perspektywy chemicznej, twarda woda to nic innego jak roztwór, w którym rozpuszczonych jest wysokie stężenie soli mineralnych, przede wszystkim tych zawierających jony wapnia i magnezu. Zrozumienie jej składu chemicznego i reakcji, w jakie wchodzi, jest kluczowe, ponieważ ma to bezpośredni wpływ na nasze codzienne życie, od efektywności detergentów po żywotność domowych urządzeń.
Twarda woda to roztwór soli mineralnych zrozum, jakie jony ją tworzą i jak wpływają na otoczenie
- Twarda woda charakteryzuje się wysokim stężeniem rozpuszczonych soli mineralnych, głównie jonów wapnia (Ca²⁺) i magnezu (Mg²⁺).
- Towarzyszące aniony to przede wszystkim wodorowęglany (HCO₃⁻), siarczany (SO₄²⁻) i chlorki (Cl⁻).
- Wyróżniamy twardość przemijającą (węglanową), którą można usunąć przez gotowanie, oraz twardość trwałą (niewęglanową), odporną na działanie temperatury.
- Głównym problemem jest powstawanie kamienia kotłowego (głównie CaCO₃) oraz obniżenie efektywności detergentów.
- Stopień twardości wody w Polsce najczęściej wyraża się w stopniach niemieckich (°dH).
- Chemiczne metody zmiękczania wody obejmują strącanie i wymianę jonową, gdzie jony Ca²⁺ i Mg²⁺ są zastępowane jonami Na⁺.
Twarda woda co to jest z perspektywy chemii?
Definicja twardości wody co tak naprawdę rozpuszcza się w Twojej kranówce?
Z chemicznego punktu widzenia, twarda woda to taka, która charakteryzuje się wysokim stężeniem rozpuszczonych soli mineralnych. Głównymi winowajcami tego zjawiska są kationy, czyli jony o ładunku dodatnim. W przeważającej mierze są to jony wapnia (Ca²⁺) i magnezu (Mg²⁺). Jednak nie tylko one wpływają na twardość. Towarzyszą im również aniony, czyli jony o ładunku ujemnym, takie jak wodorowęglany (HCO₃⁻), siarczany (SO₄²⁻), chlorki (Cl⁻) oraz azotany (NO₃⁻). To właśnie ta specyficzna mieszanka jonów nadaje wodzie jej charakterystyczne właściwości, które odczuwamy na co dzień.
Główni winowajcy: Jony wapnia (Ca²⁺) i magnezu (Mg²⁺) w roli głównej
Jony wapnia (Ca²⁺) i magnezu (Mg²⁺) są uznawane za główne przyczyny twardości wody z bardzo prostego powodu ich powszechnego występowania w środowisku naturalnym. Woda, przepływając przez warstwy gleby i skał, zwłaszcza wapiennych czy dolomitowych, rozpuszcza zawarte w nich minerały. Wapień to głównie węglan wapnia (CaCO₃), a dolomit to węglan wapnia i magnezu (CaMg(CO₃)₂). Te związki, choć słabo rozpuszczalne w czystej wodzie, w obecności dwutlenku węgla (CO₂) i wody tworzą rozpuszczalne wodorowęglany. To właśnie te jony, Ca²⁺ i Mg²⁺, mają najsilniejszy wpływ na właściwości użytkowe wody, takie jak zdolność do tworzenia osadów czy reakcje z mydłem.
Nie tylko wapń i magnez o mniej znanych jonach powodujących twardość
Chociaż wapń i magnez dominują w dyskusji o twardości wody, warto pamiętać, że inne jony metali również mogą się do niej przyczyniać, choć zazwyczaj w znacznie mniejszym stopniu. Mam tu na myśli przede wszystkim jony żelaza (Fe²⁺, Fe³⁺), manganu (Mn²⁺), a także strontu (Sr²⁺) i baru (Ba²⁺). Ich obecność w wodzie jest zazwyczaj związana z lokalnymi warunkami geologicznymi i może prowadzić do specyficznych problemów, takich jak brunatne zabarwienia wody czy osady. Jednak w kontekście ogólnej twardości wody, ich wpływ jest marginalny w porównaniu do duetu wapnia i magnezu.
Twardość wody przemijająca i trwała, czyli dwa chemiczne oblicza

Twardość przemijająca (węglanowa): Chemia kamienia w Twoim czajniku
Twardość przemijająca, często nazywana węglanową, jest zjawiskiem, które każdy z nas obserwuje w swoim czajniku. Jest ona wynikiem obecności w wodzie wodorowęglanów wapnia (Ca(HCO₃)₂) i magnezu (Mg(HCO₃)₂). Co istotne z chemicznego punktu widzenia, związki te są termicznie niestabilne. Oznacza to, że pod wpływem podwyższonej temperatury, na przykład podczas gotowania wody, ulegają rozkładowi. Ten rozkład prowadzi do wytrącania się nierozpuszczalnych osadów, które znamy jako kamień kotłowy. To właśnie dlatego po zagotowaniu twardej wody na dnie naczynia pojawia się biały nalot to namacalny dowód na zachodzącą reakcję chemiczną.
Dlaczego gotowanie pomaga? Reakcja rozkładu wodorowęglanów
Gotowanie wody jest najprostszą i najstarszą metodą usuwania twardości przemijającej. Mechanizm chemiczny jest tu bardzo klarowny. Podczas podgrzewania wodorowęglan wapnia ulega rozkładowi zgodnie z następującą reakcją:
Ca(HCO₃)₂ → CaCO₃↓ + H₂O + CO₂↑
W tej reakcji wodorowęglan wapnia (Ca(HCO₃)₂) przekształca się w nierozpuszczalny węglan wapnia (CaCO₃), który wytrąca się z roztworu w postaci stałego osadu to właśnie nasz kamień kotłowy. Dodatkowo powstaje woda (H₂O) i dwutlenek węgla (CO₂), który ulatuje w postaci gazu. Podobna reakcja zachodzi z wodorowęglanem magnezu. Dzięki temu procesowi, po zagotowaniu, woda staje się miększa, a jony wapnia i magnezu, odpowiedzialne za twardość węglanową, zostają usunięte z roztworu.
Twardość trwała (niewęglanowa): Wróg, którego gotowanie nie pokona
W przeciwieństwie do twardości przemijającej, twardość trwała, nazywana również niewęglanową, jest znacznie bardziej oporna na domowe metody zmiękczania. Jest ona spowodowana przez sole wapnia i magnezu, które nie ulegają rozkładowi pod wpływem temperatury. Oznacza to, że nawet długotrwałe gotowanie wody nie spowoduje wytrącenia się tych związków. W praktyce oznacza to, że woda z wysoką twardością trwałą nadal będzie powodować problemy, takie jak słabe pienienie się mydła czy osadzanie się kamienia, choć już nie w tak spektakularny sposób jak w przypadku twardości węglanowej.
Siarczany i chlorki cisi sprawcy trwałych problemów
Za twardość trwałą odpowiadają przede wszystkim sole wapnia i magnezu, które charakteryzują się większą stabilnością termiczną. Do najczęściej spotykanych należą siarczany wapnia (CaSO₄) i magnezu (MgSO₄), a także chlorki wapnia (CaCl₂) i magnezu (MgCl₂). Mogą to być również azotany wapnia i magnezu. Te związki, choć nie wytrącają się podczas gotowania, nadal pozostają w roztworze i mogą tworzyć osady w innych warunkach, na przykład w wyniku odparowania wody, czy też wpływać na smak wody i skuteczność detergentów. Ich obecność to cichy, ale stały problem dla instalacji i urządzeń.
Chemiczne skutki twardej wody w codziennym życiu
Tajemnica kamienia kotłowego: Jak i dlaczego osadza się na grzałkach?
Kamień kotłowy to chyba najbardziej znany i najbardziej uciążliwy skutek twardej wody. Jego powstawanie na grzałkach urządzeń AGD, takich jak pralki, zmywarki czy czajniki, jest bezpośrednio związane z opisanym wcześniej rozkładem wodorowęglanów wapnia i magnezu. Kiedy woda jest podgrzewana, rozpuszczone wodorowęglany przekształcają się w nierozpuszczalne węglany, które osadzają się na gorących powierzchniach. Te osady tworzą warstwę izolacyjną na grzałkach, co ma dwie główne negatywne konsekwencje. Po pierwsze, zmniejsza się wydajność grzewcza urządzenie musi pracować dłużej, aby osiągnąć zadaną temperaturę. Po drugie, prowadzi to do znacznego zwiększenia zużycia energii elektrycznej, co przekłada się na wyższe rachunki i niepotrzebne obciążenie dla środowiska.
Reakcja mydła z twardą wodą: Dlaczego detergenty pienią się słabiej?
Z pewnością każdy z nas zauważył, że w twardej wodzie mydło pieni się znacznie słabiej, a na powierzchni wody tworzy się nieprzyjemny osad. To również efekt reakcji chemicznych. Mydła to sole sodowe lub potasowe wyższych kwasów tłuszczowych. Kiedy jony wapnia (Ca²⁺) i magnezu (Mg²⁺) z twardej wody napotykają jony kwasów tłuszczowych z mydła, dochodzi do reakcji wymiany. Powstają wtedy nierozpuszczalne sole wapnia i magnezu kwasów tłuszczowych, potocznie nazywane "mydłami wapniowymi i magnezowymi". Te związki nie mają właściwości pianotwórczych ani myjących. Zamiast tego tworzą szary, trudny do usunięcia osad, który osadza się na skórze, włosach, tkaninach i powierzchniach sanitarnych. W efekcie musimy używać znacznie więcej detergentów, aby osiągnąć pożądany efekt czyszczenia.
Niewidoczne zagrożenie: Wpływ osadów na instalacje grzewcze i AGD
Problem kamienia kotłowego wykracza poza estetykę i efektywność energetyczną czajnika. Osady te stanowią niewidoczne, ale poważne zagrożenie dla całej domowej instalacji, zwłaszcza dla systemów grzewczych i rur. Kamień osadza się wewnątrz rur, sukcesywnie zmniejszając ich światło i utrudniając przepływ wody. Może to prowadzić do spadku ciśnienia wody, nierównomiernego ogrzewania, a w skrajnych przypadkach nawet do całkowitego zablokowania przepływu. W urządzeniach AGD, takich jak pralki czy zmywarki, kamień odkłada się nie tylko na grzałkach, ale także na elementach mechanicznych, prowadząc do ich zatarcia, uszkodzenia i w konsekwencji do awarii. Całościowo, twarda woda znacząco skraca żywotność urządzeń i zwiększa koszty ich konserwacji oraz napraw.
Jak mierzymy twardość wody stopnie niemieckie i klasyfikacja
Stopnie niemieckie (°dH) co oznaczają wartości na mapie twardości wody w Polsce?
W Polsce, podobnie jak w wielu innych krajach Europy, twardość wody najczęściej wyraża się w stopniach niemieckich (°n lub °dH). Jest to jednostka, która pozwala nam w prosty sposób porównywać twardość wody w różnych regionach. Jeden stopień niemiecki odpowiada stężeniu jonów wapnia (Ca²⁺) i magnezu (Mg²⁺) w ilości równoważnej 10 miligramom tlenku wapnia (CaO) w 1 litrze wody. To oznacza, że im wyższa wartość w °dH, tym więcej tych twardotwórczych jonów znajduje się w wodzie. Znając tę jednostkę, możemy lepiej interpretować dane dotyczące jakości wody w naszych domach i podejmować świadome decyzje dotyczące jej uzdatniania.
Od wody miękkiej do bardzo twardej: Praktyczna klasyfikacja
Aby ułatwić zrozumienie i ocenę twardości wody, przyjęto praktyczną klasyfikację, która pozwala nam szybko określić, z jakim typem wody mamy do czynienia. W Polsce, bazując na stopniach niemieckich (°dH), wyróżniamy następujące kategorie:
- woda bardzo miękka: 0-5 °dH
- woda miękka: 5-10 °dH
- woda średnio twarda: 10-15 °dH
- woda twarda: 15-20 °dH
- woda bardzo twarda: powyżej 20 °dH
Ta klasyfikacja jest dla mnie, jako eksperta, niezwykle przydatna w ocenie potencjalnych problemów i rekomendowaniu odpowiednich rozwiązań dla moich klientów. Pozwala szybko zorientować się, czy woda w danym miejscu będzie wymagała zmiękczania, czy też jej twardość mieści się w akceptowalnych normach.
Zmiękczanie wody chemiczne metody i ich mechanizmy
Metody strąceniowe: Jak zmusić jony do opuszczenia roztworu?
Chemiczne metody strąceniowe zmiękczania wody polegają na dodawaniu do niej związków chemicznych, które wchodzą w reakcję z jonami wapnia i magnezu. Celem jest utworzenie z nich nierozpuszczalnych osadów, które następnie można odfiltrować lub pozwolić im osiąść na dnie. Klasycznym przykładem jest dodawanie węglanu sodu (Na₂CO₃), znanego jako soda kalcynowana, lub wodorotlenku wapnia (Ca(OH)₂), czyli wapna gaszonego. Węglan sodu reaguje z jonami wapnia i magnezu, tworząc nierozpuszczalne węglany wapnia i magnezu. Metody te są skuteczne, ale wymagają precyzyjnego dozowania chemikaliów i często generują osady, które trzeba usunąć. Stosuje się je głównie w przemyśle lub w dużych stacjach uzdatniania wody.
Wymiana jonowa: Inteligentna pułapka na jony wapnia i magnezu
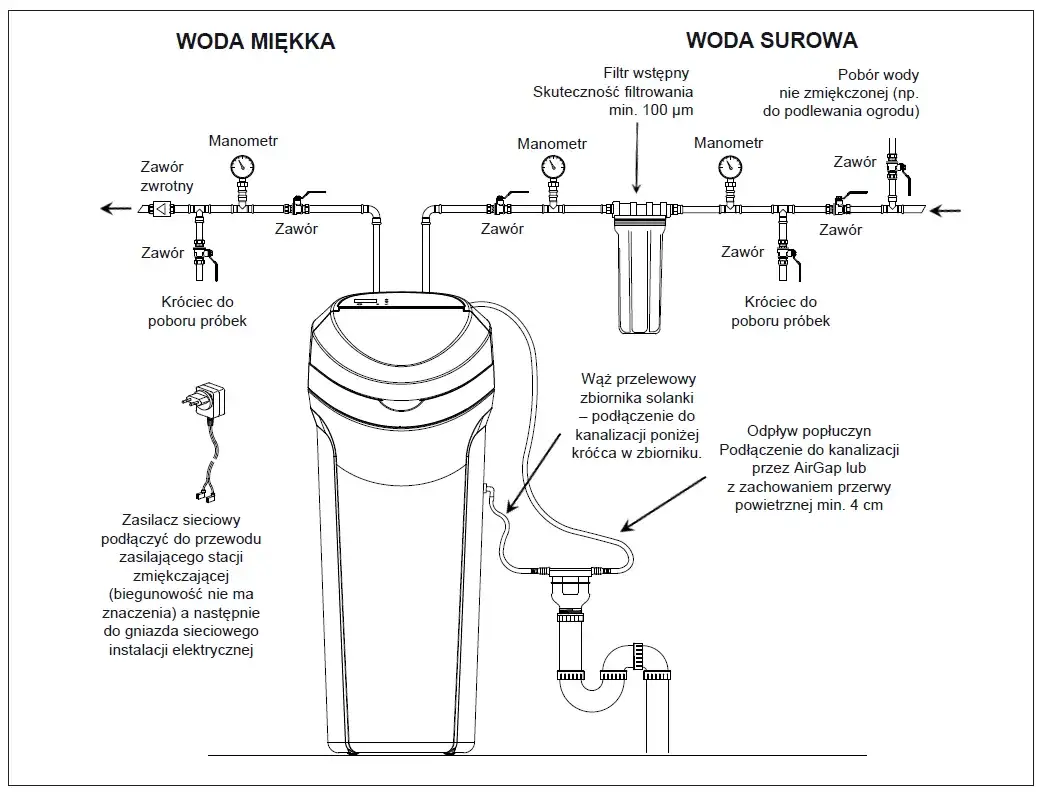
Wymiana jonowa to obecnie najpopularniejsza i najbardziej efektywna metoda zmiękczania wody, szczególnie w zastosowaniach domowych. Mechanizm działania jest genialny w swojej prostocie: woda przepływa przez specjalne złoże, zwane żywicą jonowymienną. Ta żywica zawiera jony sodu (Na⁺), które są luźno związane z jej strukturą. Kiedy jony wapnia (Ca²⁺) i magnezu (Mg²⁺) z twardej wody napotykają żywicę, są one "łapane" i wiązane przez nią, a w zamian do wody uwalniane są jony sodu. Jest to proces wymiany, gdzie szkodliwe jony Ca²⁺ i Mg²⁺ są zastępowane neutralnymi jonami Na⁺. Woda po przejściu przez zmiękczacz jest więc pozbawiona jonów odpowiedzialnych za twardość, a jej skład chemiczny jest bezpieczny dla zdrowia i urządzeń.
Rola żywic jonowymiennych i soli w domowych zmiękczaczach
Sercem każdego zmiękczacza wody jest żywica jonowymienna. To ona, dzięki swojej unikalnej strukturze chemicznej, jest w stanie selektywnie wiązać jony wapnia i magnezu. Jednak zdolność żywicy do wymiany jonów nie jest nieskończona. Z czasem złoże jonowymienne "nasyca się" jonami twardości i traci swoją skuteczność. W tym momencie niezbędna jest regeneracja. Proces ten polega na przepłukaniu złoża skoncentrowanym roztworem chlorku sodu, czyli popularnej soli tabletkowanej. Jony sodu z roztworu soli wypierają jony wapnia i magnezu z żywicy, które następnie są odprowadzane do kanalizacji. Żywica zostaje w ten sposób "naładowana" jonami sodu i jest gotowa do dalszej pracy. To właśnie dlatego regularne uzupełnianie soli w zmiękczaczu jest tak kluczowe dla jego prawidłowego funkcjonowania.
Przeczytaj również: Roztwór buforowy: Co to jest? Klucz do stabilnego pH w chemii i życiu
Twarda woda w kuchni i łazience chemiczne aspekty codziennych problemów
Zacieki i osady na szkle: Reakcje chemiczne, które widzisz na co dzień
Zacieki i osady na szklanych powierzchniach, takie jak kabiny prysznicowe, lustra czy naczynia, to najbardziej widoczne, choć często niedoceniane, chemiczne świadectwo twardej wody. Kiedy woda z kranu odparowuje, rozpuszczone w niej sole mineralne, przede wszystkim węglany wapnia i magnezu, pozostają na powierzchni. Ponieważ są to związki nierozpuszczalne w wodzie, tworzą charakterystyczne białe, matowe naloty. Proces ten jest szczególnie intensywny w łazienkach, gdzie para wodna i częste zachlapania sprzyjają szybkiemu odparowywaniu wody i wytrącaniu się osadów. Zrozumienie tego mechanizmu pomaga mi zawsze wytłumaczyć, dlaczego tak trudno jest utrzymać idealną czystość bez zmiękczania wody to po prostu chemia w działaniu!

