Osmoza to jedno z najbardziej fundamentalnych zjawisk w biologii, które rządzi życiem na poziomie komórkowym i ma kluczowe znaczenie dla funkcjonowania wszystkich organizmów. Zrozumienie tego procesu jest absolutnie niezbędne, aby pojąć, jak rośliny pobierają wodę, jak nasze komórki utrzymują równowagę, a nawet jak działają niektóre technologie codziennego użytku.
Osmoza to kluczowy proces transportu wody fundament życia komórkowego
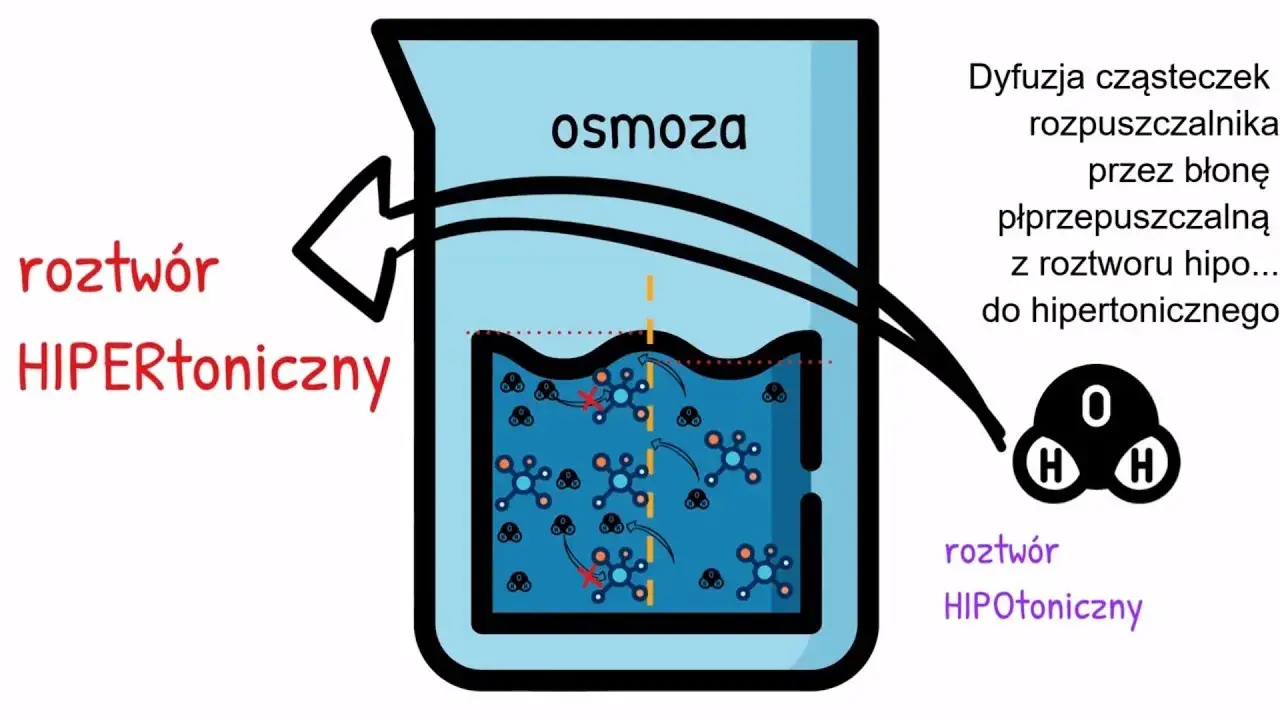
- Osmoza to spontaniczny ruch wody przez błonę półprzepuszczalną, dążący do wyrównania stężeń roztworów.
- Kluczowe dla osmozy są: błona półprzepuszczalna, różnica stężeń substancji rozpuszczonych oraz potencjał wody.
- W zależności od stężenia roztworu, komórki mogą pęcznieć (roztwór hipotoniczny), kurczyć się (roztwór hipertoniczny) lub pozostawać w równowadze (roztwór izotoniczny).
- Proces ten jest niezbędny dla życia odpowiada za pobieranie wody przez rośliny, utrzymanie ich jędrności (turgor) oraz regulację gospodarki wodnej u zwierząt (osmoregulacja).
- Osmoza ma również praktyczne zastosowania, m.in. w konserwacji żywności czy technologii uzdatniania wody (odwrócona osmoza).
Definicja osmozy, którą zrozumie każdy bez skomplikowanego żargonu
W najprostszych słowach, osmoza to spontaniczny ruch wody (lub innego rozpuszczalnika) przez specjalną błonę, zwaną błoną półprzepuszczalną. Ten ruch odbywa się zawsze z miejsca, gdzie stężenie substancji rozpuszczonej jest niższe (czyli jest więcej "wolnej" wody), do miejsca, gdzie stężenie substancji rozpuszczonej jest wyższe (czyli jest mniej "wolnej" wody). Celem tego procesu jest dążenie do wyrównania stężeń po obu stronach błony. W biologii, gdy mówimy o osmozie, niemal zawsze mamy na myśli ruch wody, która jest najważniejszym rozpuszczalnikiem w organizmach żywych.
Osmoza a dyfuzja: Dlaczego tych pojęć nie można używać zamiennie?
Często widzę, że te dwa pojęcia są ze sobą mylone, a to błąd! Dyfuzja to ogólny termin opisujący ruch cząsteczek z obszaru o wyższym stężeniu do obszaru o niższym stężeniu, dążący do ich równomiernego rozmieszczenia. Może dotyczyć gazów, cieczy, a także substancji rozpuszczonych w wodzie. Osmoza jest natomiast specyficznym rodzajem dyfuzji, która dotyczy wyłącznie ruchu rozpuszczalnika (wody) i zawsze odbywa się przez błonę półprzepuszczalną. To właśnie obecność tej błony i jej selektywne właściwości są kluczową różnicą, która odróżnia osmozę od ogólnej dyfuzji.
Trzy filary osmozy: Rola błony półprzepuszczalnej, stężenia i potencjału wody
Aby osmoza mogła zajść, potrzebujemy trzech podstawowych elementów, które działają ze sobą w skoordynowany sposób.
Pierwszym z nich jest błona półprzepuszczalna. Jej rola jest absolutnie fundamentalna. Błona ta działa jak selektywny filtr pozwala na swobodny przepływ cząsteczek wody, ale jednocześnie zatrzymuje większość większych cząsteczek substancji rozpuszczonych. W komórkach biologiczną błoną półprzepuszczalną jest oczywiście błona komórkowa, która otacza każdą żywą komórkę, kontrolując, co do niej wchodzi, a co wychodzi.
Drugim elementem jest różnica stężeń, czyli gradient stężeń. To właśnie ta różnica w ilości substancji rozpuszczonych po obu stronach błony jest siłą napędową osmozy. Woda zawsze będzie dążyć do tego, aby rozcieńczyć roztwór o wyższym stężeniu, przenosząc się do niego z roztworu o niższym stężeniu, aż do momentu, gdy stężenia się wyrównają lub zostanie osiągnięta równowaga.
Trzeci filar to potencjał wody. To pojęcie może brzmieć skomplikowanie, ale w gruncie rzeczy jest to miara zdolności wody do przemieszczania się. Woda zawsze płynie z obszaru o wyższym potencjale wody do obszaru o niższym potencjale. Czysta woda ma najwyższy potencjał (przyjmuje się, że wynosi on zero), a dodanie do niej substancji rozpuszczonych zawsze obniża ten potencjał. Warto też wspomnieć o ciśnieniu osmotycznym to siła, jaką trzeba by przyłożyć do roztworu, aby powstrzymać napływ wody przez błonę półprzepuszczalną. Im wyższe stężenie roztworu, tym wyższe ciśnienie osmotyczne.
Komórka w wodnym świecie: wpływ różnych roztworów na jej przetrwanie
To, w jakim środowisku wodnym znajdzie się komórka, ma dla niej ogromne znaczenie. W zależności od stężenia substancji rozpuszczonych w otaczającym ją roztworze, komórka może reagować na trzy główne sposoby.
Roztwór izotoniczny: Stan idealnej równowagi dla komórki
Roztwór izotoniczny to taki, w którym stężenie substancji rozpuszczonych jest takie samo jak wewnątrz komórki. W takiej sytuacji woda swobodnie przepływa przez błonę komórkową w obu kierunkach do wnętrza komórki i na zewnątrz ale dzieje się to w równych ilościach. Oznacza to, że komórka nie zmienia swojej objętości, zachowuje swój kształt i znajduje się w stanie idealnej równowagi. Dla wielu komórek zwierzęcych, w tym ludzkich, takie środowisko jest optymalne do funkcjonowania.
Roztwór hipotoniczny: Co się dzieje, gdy komórka pęcznieje jak balon?
Kiedy komórka znajdzie się w roztworze hipotonicznym, oznacza to, że stężenie substancji rozpuszczonych w otoczeniu jest niższe niż w jej wnętrzu. Zgodnie z zasadami osmozy, woda zaczyna masowo napływać do komórki, dążąc do wyrównania stężeń. W przypadku komórek zwierzęcych, które nie posiadają sztywnej ściany komórkowej, nadmierny napływ wody może doprowadzić do ich pęcznienia, a w końcu do pęknięcia, czyli tak zwanej hemolizy (w przypadku krwinek czerwonych). Komórki roślinne reagują inaczej napływ wody powoduje wzrost ciśnienia wewnątrz komórki, które naciska na ścianę komórkową, prowadząc do stanu turgoru, czyli jędrności. Roślina staje się sztywna i wyprostowana.
Roztwór hipertoniczny: Dramat kurczącej się komórki, czyli czym jest plazmoliza i krenacja
Sytuacja w roztworze hipertonicznym jest odwrotna. Tutaj stężenie substancji rozpuszczonych w otoczeniu jest wyższe niż wewnątrz komórki. Woda, dążąc do wyrównania stężeń, zaczyna intensywnie wypływać z komórki. Dla komórek zwierzęcych utrata wody prowadzi do ich kurczenia się i marszczenia, co nazywamy krenacją. Komórki roślinne również tracą wodę, ale ze względu na obecność sztywnej ściany komórkowej, nie kurczą się całościowo. Zamiast tego, protoplast (czyli żywa część komórki, wraz z błoną komórkową) odrywa się od ściany komórkowej i kurczy się do środka. To zjawisko nazywamy plazmolizą.
Komórka roślinna kontra zwierzęca kto lepiej radzi sobie ze zmianami stężeń?
Jak widać, komórki roślinne i zwierzęce, choć obie podlegają osmozie, radzą sobie ze zmianami stężeń w otoczeniu w nieco odmienny sposób. Główna różnica wynika z obecności sztywnej ściany komórkowej u roślin. To ona chroni komórkę roślinną przed pęknięciem w środowisku hipotonicznym, pozwalając na rozwinięcie turgoru, który jest dla rośliny wręcz pożądany.
Z drugiej strony, brak ściany komórkowej sprawia, że komórki zwierzęce są znacznie bardziej wrażliwe na zmiany osmotyczne. Zarówno nadmierny napływ wody (hemoliza), jak i jej utrata (krenacja) mogą być dla nich śmiertelne. Dlatego też organizmy zwierzęce, w tym ludzie, wykształciły złożone mechanizmy osmoregulacji, aby precyzyjnie kontrolować stężenie płynów ustrojowych i chronić swoje komórki przed uszkodzeniami osmotycznymi.
Osmoza dlaczego jest niezbędna do życia?
Osmoza to nie tylko ciekawostka naukowa, ale fundamentalny proces, bez którego życie, jakie znamy, nie mogłoby istnieć. Odgrywa kluczową rolę w wielu aspektach funkcjonowania organizmów.
Jak rośliny "piją" wodę? Osmotyczna siła napędowa natury
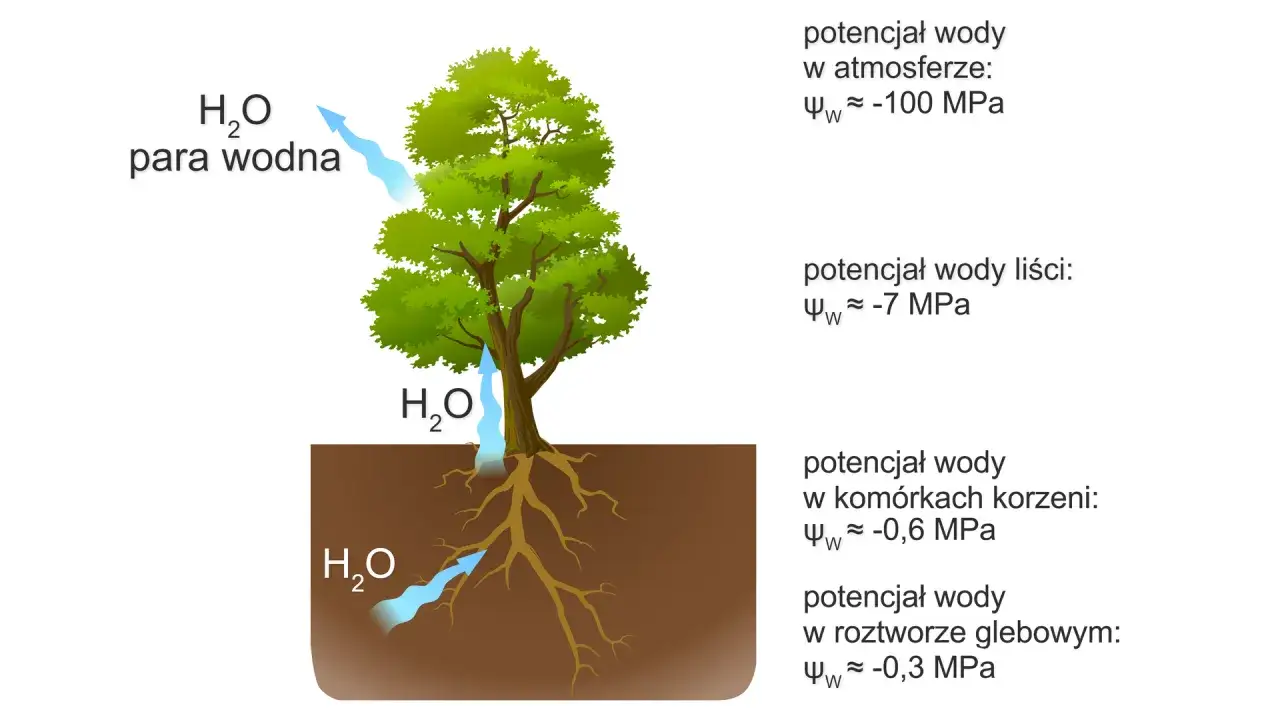
Jednym z najbardziej spektakularnych przykładów działania osmozy jest sposób, w jaki rośliny pobierają wodę z gleby. Gleba zazwyczaj stanowi roztwór hipotoniczny w stosunku do komórek korzeni. Oznacza to, że stężenie substancji rozpuszczonych w komórkach korzeni jest wyższe niż w wodzie glebowej. Dzięki temu gradientowi stężeń woda, na drodze osmozy, aktywnie wnika do komórek korzeni, a następnie jest transportowana wyżej, do pozostałych części rośliny. To osmotyczna siła napędowa umożliwia roślinom "picie" i utrzymanie życia.
Turgor, czyli wewnętrzny szkielet rośliny jak osmoza utrzymuje je w pionie?
Wspomniany już turgor to nic innego jak ciśnienie, jakie protoplast komórki roślinnej wywiera na jej ścianę komórkową, gdy jest ona w pełni nawodniona. Dzięki osmozie woda napływa do komórek roślinnych, zwiększając ich wewnętrzne ciśnienie. To właśnie turgor nadaje roślinom sztywność i jędrność, pełniąc rolę swoistego "wewnętrznego szkieletu". Bez turgoru rośliny więdną i tracą zdolność do utrzymania pionowej pozycji, co jest kluczowe dla ich wzrostu, fotosyntezy i ogólnego przetrwania.
Osmoregulacja: Wewnętrzny termostat wodny u zwierząt i ludzi
Dla zwierząt, w tym ludzi, kluczowe jest utrzymanie stałego ciśnienia osmotycznego płynów ustrojowych, niezależnie od zmian w otoczeniu czy spożywanej diecie. Ten proces nazywamy osmoregulacją. To zdolność organizmu do aktywnego kontrolowania bilansu wodnego i stężenia soli, co jest niezbędne dla prawidłowego funkcjonowania komórek i tkanek. Ryby słodkowodne, słonowodne, a także my sami, musimy nieustannie regulować swoją gospodarkę wodną, aby nasze komórki nie pęczniały ani nie kurczyły się nadmiernie. Bez skutecznej osmoregulacji przetrwanie w zmiennym środowisku byłoby niemożliwe.
Rola osmozy w pracy Twoich nerek cichy bohater organizmu
W ludzkim organizmie osmoza odgrywa absolutnie fundamentalną rolę w pracy nerek naszych naturalnych filtrów. Nerki wykorzystują różnice ciśnień osmotycznych do filtracji krwi i reabsorpcji wody oraz niezbędnych substancji z powrotem do krwiobiegu. Dzięki temu procesowi jesteśmy w stanie pozbywać się toksyn i nadmiaru wody, jednocześnie zatrzymując cenne składniki. To właśnie osmoza umożliwia utrzymanie precyzyjnej równowagi wodno-elektrolitowej, która jest kluczowa dla zdrowia i życia.
Osmoza na co dzień: gdzie spotykasz to zjawisko?
Osmoza to nie tylko skomplikowany proces biologiczny, ale zjawisko, które ma swoje praktyczne zastosowania i objawia się w wielu codziennych sytuacjach. Warto zwrócić na nie uwagę!
Dlaczego posypanie ślimaka solą jest dla niego zabójcze? Brutalna lekcja osmozy
To drastyczny, ale bardzo obrazowy przykład działania osmozy. Kiedy posypujemy ślimaka solą, na jego powierzchni tworzy się roztwór o bardzo wysokim stężeniu (hipertoniczny). Ponieważ stężenie wewnątrz komórek ślimaka jest znacznie niższe, woda zaczyna masowo wypływać z jego ciała na zewnątrz, zgodnie z zasadami osmozy. Ślimak gwałtownie się odwadnia, co prowadzi do jego śmierci. To brutalna, ale skuteczna demonstracja siły osmotycznej.
Konserwowanie żywności: Jak cukier i sól wykorzystują osmozę do walki z bakteriami
Sól i cukier to jedne z najstarszych i najskuteczniejszych środków konserwujących żywność, a ich działanie opiera się właśnie na osmozie. Dodając duże ilości soli (np. do mięsa) lub cukru (np. do owoców w dżemie), tworzymy wokół żywności środowisko hipertoniczne. Kiedy bakterie lub grzyby próbują skolonizować taką żywność, woda z ich komórek jest "wyciągana" na zewnątrz przez osmozę. Odwodnione mikroorganizmy nie są w stanie rozwijać się i rozmnażać, co skutecznie zapobiega psuciu się jedzenia. To sprytne wykorzystanie biologii w kuchni!
Odwrócona osmoza: Jak ta technologia zapewnia nam czystą wodę w filtrach?
Odwrócona osmoza to fascynująca technologia, która "odwraca" naturalny proces osmozy. Zamiast czekać, aż woda przepłynie z niższego do wyższego stężenia, w odwróconej osmozie aplikuje się zewnętrzne ciśnienie na roztwór o wyższym stężeniu. To ciśnienie zmusza cząsteczki wody do przepływu przez półprzepuszczalną membranę w kierunku przeciwnym do naturalnego gradientu, pozostawiając za sobą zanieczyszczenia, sole mineralne i inne substancje rozpuszczone. Technologia ta jest szeroko stosowana w domowych filtrach do wody, w przemyśle do odsalania wody morskiej, a także w medycynie do dializ. Dzięki niej możemy cieszyć się czystą i bezpieczną wodą.
Osmoza fundamentalny proces kształtujący życie
Najważniejsze wnioski: Co musisz zapamiętać o osmozie?
- Osmoza to ruch wody przez błonę półprzepuszczalną, z roztworu o niższym stężeniu substancji rozpuszczonej do wyższego.
- Kluczowe dla jej przebiegu są: błona półprzepuszczalna, różnica stężeń i potencjał wody.
- W zależności od otoczenia, komórki mogą pęcznieć (hipotoniczny), kurczyć się (hipertoniczny) lub być w równowadze (izotoniczny).
- Jest niezbędna dla życia: odpowiada za pobieranie wody przez rośliny, utrzymanie ich turgoru oraz osmoregulację u zwierząt.
- Ma praktyczne zastosowania, np. w konserwacji żywności i technologii uzdatniania wody (odwrócona osmoza).
Przeczytaj również: Dlaczego woda jest fundamentem życia? Unikalne właściwości H₂O
Dlaczego zrozumienie osmozy pozwala lepiej pojąć całą biologię?
Zrozumienie osmozy to jak posiadanie klucza do wielu drzwi w biologii. Ten proces jest tak wszechobecny i fundamentalny, że bez jego znajomości trudno byłoby pojąć, jak funkcjonują pojedyncze komórki, jak rośliny utrzymują swoją strukturę, dlaczego zwierzęta potrzebują nerek, czy nawet jak możemy wykorzystać procesy biologiczne do konserwacji żywności. Osmoza to jeden z tych mechanizmów, które pokazują, jak proste prawa fizyczne i chemiczne leżą u podstaw złożoności życia na Ziemi.